Química (términos griegos
χημία o χημεία, quemia y quemeia) es la ciencia que estudia
tanto la composición, estructura y propiedades de la materia como los cambios
que ésta experimenta durante las reacciones químicas y su relación con la
energía. Es definida, en tanto, por Linus Pauling, como la ciencia que estudia
las sustancias, su estructura (tipos y formas de acomodo de los átomos), sus
propiedades y las reacciones que las transforman en otras sustancias. La química moderna se fue formulando a partir de la
alquimia, una práctica proto-científica de carácter filosófico, que combina
elementos de la química, la metalurgia, la física, la medicina, la biología,
entre otras ciencias y artes. Esta fase termina al ocurrir la llamada,
Revolución de la química, basada en la ley de conservación de la masa y la
teoría de la oxígeno-combustión postuladas por el científico francés, Antoine
Lavoisier. Las disciplinas de la química se agrupan según la clase de
materia bajo estudio o el tipo de estudio realizado. Entre éstas se tienen la
química inorgánica, que estudia la materia inorgánica; la química orgánica, que
estudia la materia orgánica; la bioquímica, que estudia las substancias
existentes en organismos biológicos; la físico-química, que comprende los
aspectos energéticos de sistemas químicos a escalas macroscópicas, moleculares
y atómicas, o la química analítica, que analiza muestras de materia y trata de
entender su composición y estructura.
¿QUE ES ALQUIMIA?
En la historia de la ciencia, la alquimia (del árabe الخيمياء [al-khīmiyā]) es una
antigua práctica proto-científica y una disciplina filosófica que combina
elementos de la química, la metalurgia, la física, la medicina, la astrología,
la semiótica, el misticismo, el espiritualismo y el arte. La alquimia fue
practicada en Mesopotamia, el Antiguo Egipto, Persia, la India y China, en la
Antigua Grecia y el Imperio romano, en el Imperio islámico y después en Europa
hasta el siglo XVIII, en una compleja red de escuelas y sistemas filosóficos
que abarca al menos 2 500 años.
La alquimia occidental ha estado siempre estrechamente
relacionada con el hermetismo, un sistema filosófico y espiritual que tiene sus
raíces en Hermes Trimegisto, una deidad sincrética greco-egipcia y legendario
alquimista. Estas dos disciplinas influyeron en el nacimiento del rosacrucismo,
un importante movimiento esotérico del siglo XVII. En el transcurso de los
comienzos de la época moderna, la alquimia dominante evolucionó en la actual química.
Actualmente es de interés para los historiadores de la
ciencia y la filosofía, así como por sus aspectos místicos, esotéricos y
artísticos. La alquimia fue una de las principales precursoras de las ciencias
modernas, y muchas de las sustancias, herramientas y procesos de la antigua
alquimia han servido como pilares fundamentales de las modernas industrias
químicas y metalúrgicas.
Aunque la alquimia adopta muchas formas, en la cultura
popular es citada con mayor frecuencia en historias, películas, espectáculos y
juegos como el proceso usado para transformar plomo (u otros elementos) en oro.
Otra forma que adopta la alquimia es la de la búsqueda de la piedra filosofal,
con la que se era capaz de lograr la habilidad para transmutar oro o la vida
eterna.
En el plano espiritual de la alquimia, los alquimistas
debían transmutar su propia alma antes de transmutar los metales. Esto quiere
decir que debían purificarse, prepararse mediante la oración y el ayuno.
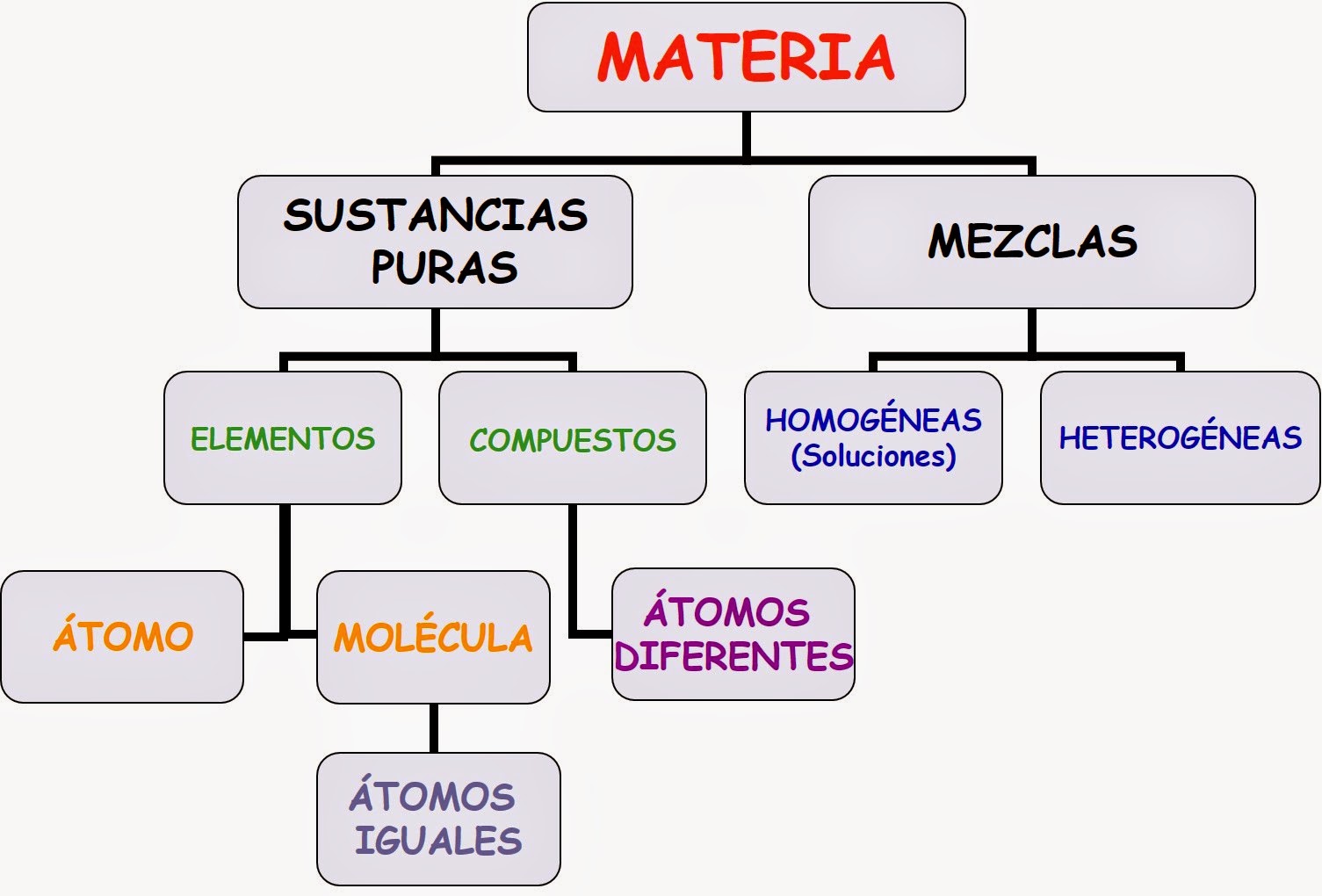
2.-¿QUE ES MATERIA?
Materia es todo aquello que ocupa un lugar en el espacio. Estados de la materia: solido, líquido y gaseoso. Al transformarse optan por ciertas propiedades. Las propiedades generales son aquellas que poseen todos los tipos de materia y por eso nos permiten saber qué cosas son materias y que cosas no lo son, como el volumen, la masa, la inercia, etc. Las propiedades son características o particularidades son aquellos atributos que nos permiten distinguir un tipo de materia y de otro, como la densidad, ductilidad, solubilidad, dureza, etc
ELEMENTO
MEZCLA HOMOGÉNEA
MEZCLA HETEROGÉNEA
Un elemento químico es un tipo de materia constituida por
átomos de la misma clase. En su forma más simple posee un número determinado de
protones en su núcleo, haciéndolo pertenecer a una categoría única clasificada
con el número atómico, aun cuando este pueda desplegar distintas masas
atómicas. Es un átomo con características físicas únicas, aquella sustancia que
no puede ser descompuesta mediante una reacción química, en otras más simples.
No existen dos átomos de un mismo elemento con características distintas y, en
el caso de que estos posean número másico distinto, pertenecen al mismo
elemento pero en lo que se conoce como uno de sus isótopos. También es
importante diferenciar entre un «elementos químicos» de una sustancia simple.
Los elementos se encuentran en la tabla periódica de los elementos.
El ozono (O3) y el dioxígeno (O2) son dos sustancias
simples, cada una de ellas con propiedades diferentes. Y el elemento químico
que forma estas dos sustancias simples es el oxígeno (O). Otro ejemplo es el
elemento químico carbono, que se presenta en la naturaleza como grafito o como
diamante (estados alotrópicos).
Algunos elementos se han encontrado en la naturaleza y otros
obtenidos de manera artificial, formando parte de sustancias simples o de
compuestos químicos. Otros han sido creados artificialmente en los aceleradores
de partículas o en reactores atómicos. Estos últimos suelen ser inestables y
sólo existen durante milésimas de segundo. A lo largo de la historia del
universo se han ido generando la variedad de elementos químicos a partir de
nucleosíntesis en varios procesos, fundamentalmente debidos a estrellas.
Los nombres de los elementos químicos son nombres comunes y
como tales deben escribirse sin mayúscula inicial, salvo que otra regla
ortográfica lo imponga.
En química, un compuesto es una sustancia formada por la
unión de dos o más elementos de la tabla periódica. Una característica esencial
es que tiene una fórmula química. Por ejemplo, el agua es un compuesto formado
por hidrógeno y oxígeno en la razón de 2 a 1 (en número de átomos): H2O
En general, esta razón es debida a una propiedad intrínseca
(ver valencia). Un compuesto está formado por moléculas o iones con enlaces
estables y no obedece a una selección humana arbitraria. Por este motivo el
bronce o el chocolate son denominadas mezclas o aleaciones, pero no compuestos.
Los elementos de un compuesto no se pueden dividir o separar
por procesos físicos (decantación, filtración, destilación, etcétera), sino
sólo mediante procesos químicos.
MEZCLA
Una
mezcla es un sistema material formado por dos o más componentes unidos, pero no
combinados químicamente. En una mezcla no ocurre una reacción química y cada
uno de sus componentes mantiene su identidad y propiedades químicas. No
obstante, algunas mezclas pueden ser reactivas, es decir, que sus componentes
pueden reaccionar entre sí en determinadas condiciones ambientales, como una
mezcla aire-combustible en un motor de combustión interna.
Es
la combinación física de dos o más sustancias que retienen sus identidades y
que se mezclan pudiendo formar según sea el caso aleaciones, soluciones, suspensiones
y coloides.
Son
el resultado del mezclado mecánico de sustancias químicas tales como elementos
y compuestos, sin que existan enlaces químicos u otros cambios químicos, de
forma tal que cada sustancia ingrediente mantiene sus propias propiedades químicas.1
A pesar de que no se producen cambios químicos de sus componentes, las
propiedades físicas de una mezcla, tal como por ejemplo su punto de fusión,
pueden ser distintas de las propiedades de sus componentes. Algunas mezclas se
pueden separar en sus componentes mediante procesos físicos (mecánicos o
térmicos), como ser destilación, disolución, separación magnética, flotación,
filtración, decantación o centrifugación. Los azeótropos son un tipo de mezcla
que por lo general requiere de complicados procesos de separación para obtener
sus componentes.
Si
después de mezclar algunas sustancias, éstas reaccionan químicamente, entonces
no se pueden recuperar por medios físicos, pues se han formado compuestos
nuevos.
MEZCLA HOMOGÉNEA
Las mezclas homogéneas son aquellas en las que los
componentes de la mezcla no son identificables a simple vista. Una mezcla
homogénea importante de nuestro planeta es el aire. El aire está formado por
varios componentes como:
-Oxígeno: Elemento O.
-Nitrógeno: Elemento N.
-Dióxido de carbono: Compuesto CO2
-Vapor de agua
-Otros gases en menor cantidad.
Entre las mezclas homogéneas se distingue un tipo especial
denominado disolución o solución. Al componente que se encuentra en mayor
cantidad se le denomina solvente o disolvente y al que se encuentra en menor
cantidad, soluto.MEZCLA HETEROGÉNEA
Una mezcla heterogénea es aquella que posee una composición
no uniforme en la cual se pueden distinguir a simple vista sus componentes y
está formada por dos o más sustancias, físicamente distintas, distribuidas en
forma desigual. Las partes de una mezcla heterogénea pueden separarse
fácilmente. Pueden ser gruesas o suspensiones de acuerdo al tamaño. Mezclas
gruesas: El tamaño de las partículas es apreciable,por ejemplo: las ensaladas,
concreto, etc. Y suspensiones: Las partículas se depositan con el tiempo, por
lo general tiene la leyenda "agitese bien antes de usar", por
ejemplo: medicamentos, aceite con agua, etc.
Dispersión coloidal
En química un coloide, suspensión coloidal o dispersión
coloidal es un sistema fisicoquímico formado por dos o más fases,
principalmente: una continua, normalmente fluida, y otra dispersa en forma de
partículas; por lo general sólidas. La fase dispersa es la que se halla
proporcionalmente en menor cantidad. La mezcla heterogénea no es visible a
nivel macroscópico, sin embargo con la ayuda de una microscopio es posible
distinguir sus componentes y apreciar que se trata de una mezcla heterogénenea.
Suspensión química
Suspensión se denomina a las mezclas que tienen partículas
finas suspendidas en un líquido durante un tiempo y luego se sedimentan. En la
fase inicial se puede ver que el recipiente contiene elementos distintos. Se
pueden separar por medios físicos. Algunos ejemplos de suspensiones son el
engrudo (agua con harina) y la mezcla de agua con aceite.