El nombre «átomo» proviene del latín atomum, y este del
griego ἄτομον 'sin porciones, indivisible'; también, se deriva de a- ('no') y
tómo (divisible).1 El concepto de átomo como bloque básico e indivisible que
compone la materia del universo fue postulado por la escuela atomista en la
Antigua Grecia. Sin embargo, no fueron considerados seriamente por los
científicos hasta el siglo XIX, cuando fueron introducidos para explicar
ciertas leyes químicas. Con el desarrollo de la física nuclear en el siglo XX
se comprobó que el átomo puede subdividirse en partículas más pequeñas.
Los átomos son objetos muy pequeños con masas igualmente
minúsculas: su diámetro y masa son del orden de la billonésima parte de un
metro y cuatrillonésima parte de un gramo. Solo pueden ser observados mediante
instrumentos especiales tales como un microscopio de efecto túnel. Más de un
99,94 % de la masa del átomo está concentrada en su núcleo, en general
repartida de manera aproximadamente equitativa entre protones y neutrones. El
núcleo de un átomo puede ser inestable y sufrir una transmutación mediante
desintegración radioactiva. Los electrones en la nube del átomo están
repartidos en distintos niveles de energía u orbitales, y determinan las
propiedades químicas del mismo. Las transiciones entre los distintos niveles
dan lugar a la emisión o absorción de radiación electromagnética en forma de
fotones, y son la base de la espectroscopia.
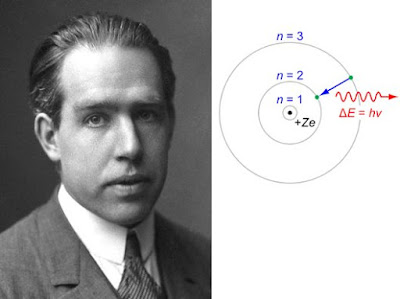 |
| Bohr y su modelo del átomo de Hidrógeno. |
El átomo es un constituyente de la materia ordinaria, con
propiedades químicas bien definidas, formado a su vez por constituyentes más
elementales sin propiedades químicas bien definidas. Cada elemento químico está
formado por átomos del mismo tipo (con la misma estructura electrónica básica),
y que no es posible dividir mediante procesos químicos.
Los átomos se clasifican de acuerdo al número de protones y
neutrones que contenga su núcleo. El número de protones o número atómico
determina su elemento químico, y el número de neutrones determina su isótopo.
Un átomo con el mismo número de protones que de electrones es eléctricamente
neutro. Si por el contrario posee un exceso de protones o de electrones, su
carga neta es positiva o negativa, y se denomina ion.
2.-EL ÁTOMO NUCLEAR
No hay comentarios:
Publicar un comentario